- Трішки історії
- Закон природи, який не можна відкрити без термометра
- Ще трохи історії
- Про молекулярний хаос і про його законах
- Про температурних шкалах
- Газовий термометр і абсолютна шкала температур
- Що ж таке температура?
- Чи потрібна величина, яка називається температурою?
Кикоин А. Температура, теплота, термометр // Квант. - 1990. - № 8. - С. 10-19.
За спеціальною домовленістю з редколегією та редакцією журналу "Квант"
Температура - одна з тих не надто багатьох фізичних величин, про які людина дізнається не тільки до того, як почне вивчати фізику, а й до того, як навчиться грамоти. Уже в ранньому дитинстві ми дізнаємося, що словами гаряче, тепле, холодне, що відображає наші відчуття, відповідають різні значення температури. Ми чуємо про те, що влітку температура висока, а взимку низька, що у здорової людини температура тіла 36,6 градуса, а якщо вона вище, то потрібно викликати лікаря ...
Через звичності поняття температури ми зазвичай не віддаємо собі звіту в тому, наскільки ця величина своєрідна, наскільки вона відрізняється від інших звичних величин, таких як довжина, маса, обсяг. А відмінність тут дуже істотне. Складається воно ось у чому.
Якщо з'єднати десять стрижнів довжиною в 1 м кожен, приставивши їх один до іншого, то вийде стрижень довжиною в 10 м. Десять мас в 1 кг кожна в сумі дадуть масу в 10 кг і т. Д. Але якщо з'єднати десять тіл, кожне з яких має температуру 20 градусів, то ми отримаємо тіло, температура якого 20 градусів, а не 200. температури тіл при їх з'єднанні не складаються, як складаються їхні довжини, обсяги, маси і т. д. Довжина в 100 м - ця сума ста довжин в 1 м, але температура в 100 градусів - це не сума ста температур в 1 градус кожна, подібно до того, як людина в озрасте 15 років - це не те ж саме, що 15 однорічних дітей! Температура, як кажуть, величина не аддитивная. У цьому - одна з найважливіших особливостей цієї величини.
З цією особливістю пов'язаний і спосіб вимірювання температури. Щоб виміряти довжину тіла, потрібно порівняти його з іншим тілом, довжина якого прийнята за одиницю. Визначити масу тіла - значить порівняти її з іншою масою, прийнятої за одиницю. Адже і довжина, і маса тіла дорівнюють відповідно сумі довжин і мас його частин.
Але температуру так виміряти не можна. Але це означає, що сама величина температури взагалі не може бути виміряна, раз її не можна порівнювати з еталоном температури. Яким же чином температуру все-таки вимірюють?
Трішки історії
Прилад для вимірювання температури - термометр - вперше був винайдений Галілеєм близько 1592 роки (саме слово «термометр» вперше зустрічається в літературі в 1624 році). Спосіб вимірювання температури, запропонований Галілеєм, принципово не відрізняється від того, яким користуються і в наш час.
Схема придуманого ним приладу показана на малюнку 1.
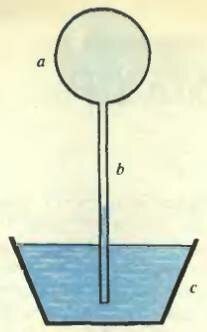
Мал. 1
Невеликий скляний балон (a) припаяний до тонкої довгій трубці (b) з відкритим кінцем. Балон нагрівають руками і занурюють нижній кінець трубки в посудину з водою (c). У міру того як балон охолоджується до температури навколишнього повітря, рівень води в трубці піднімається над рівнем води в посудині.
Легко зрозуміти, що в приладі Галілея використовується той факт, що обсяг газу в балоні з трубкою залежить від температури. Тому щодо зміни обсягу газу можна судити і про зміну температури.
Звичайно, описаний прилад ще не термометр. По ньому можна відраховувати числове значення температури. Тому його слід називати не термометром, а термоскопом. Але якщо термоскоп тим чи іншим способом забезпечити шкалою, то він стане термометром. На вирішення цього завдання потрібно майже 150 років. Поки для нас важливо, що вже в приладі Галілея міститься принцип вимірювання температури, і принцип цей не довелося змінювати аж до наших днів: температура безпосередньо не вимірюється. Вимірюється величина, що залежить від температури. У термоскопе Галілея такою величиною був обсяг газу. У сучасному ртутному термометрі величиною, що залежить від температури, зі зміни якою судять про зміну температури, теж є обсяг, але не газу, а ртуті. Поряд з обсягом газу такою величиною може бути тиск газу (при постійному обсязі), довжина твердого стрижня, електричний опір провідника і т. Д.
Закон природи, який не можна відкрити без термометра
Уже перші недосконалі термометри і навіть термоскопа дозволили відкрити один з найважливіших законів природи - закон теплового рівноваги. Закон цей багатьом здається і здавався настільки очевидним, що на його відкриття не претендує жоден учений і ніхто не може вказати дати його відкриття. Складається цей закон в тому, що будь-яка ізольована група (система) тел сама собою з плином часу приходить в стан, при якому температури всіх тіл системи однакові. Такий стан і називається станом теплового рівноваги.
Ясно, що закон теплового рівноваги міг бути відкритий тільки після винаходу термометра. З іншого боку, саме вимірювання температури за допомогою термометра засноване на законі теплового рівноваги. Адже термометр теж тіло, що має певну температуру. І він вимірює саме власну температуру. А якщо ми хочемо з його допомогою виміряти температуру якогось іншого тіла, воно повинно бути в тепловій рівновазі з термометром, тому що в цьому випадку температури тіла і термометра однакові. Ось чому при вимірюванні температури тіла за допомогою термометра завжди доводиться чекати деякий час - чекати встановлення теплової рівноваги між тілом і термометром.
Ще трохи історії
Отже, термоскоп з'явився в кінці XVI століття. Термометром він став приблизно в середині XVIII століття. Але що саме вимірює термометр? Що таке температура? Правильна відповідь на це питання була дана ще через сто років після того, як з'явився термометр.
Температура - величина, яка характеризує тепловий стан тіла. Про холодних і гарячих тілах ми говоримо, що у них різна температура. Отже, питання про те, що таке температура, зводиться до питання: чим відрізняється холодне тіло від гарячого?
Перший відповідь на це питання дав сам Галілей. З того легко спостережуваного факту, що якщо поблизу гарячого тіла знаходиться холодне, то гаряче тіло охолоджується, а холодну нагрівається, Галілей зробив природний висновок, що від гарячого тіла до холодного щось переходить (з таким же правом можна було вважати, що щось то переходить від холодного до гарячого!). Галілей вважав, що це «щось» є особливе теплове речовина. І більшість дослідників XVII-XVIII століть дотримувалися такої ж точки зору і називали це речовина теплорода.
Відповідно до теорії, заснованої на уявленні про теплорода, гаряче тіло відрізняється від холодного тим, що в ньому більше теплорода, ніж в холодному. Встановлення теплового рівноваги за цим поданням полягає в тому, що теплород переходить від гарячого тіла до холодного. Значить, будь-яке тіло складається ніби з двох речовин - речовини самого тіла (вода, мідь, залізо, скло) і теплорода. Кожне тіло - це суміш речовини тіла і речовини теплоти (теплорода). Слово «температура» якраз і означає суміш. І протягом майже півтора століття вважалося, що вимірюючи температуру, ми вимірюємо концентрацію теплорода в тілі. Звідси і назва одиниці температури - градус. Саме в таких одиницях вимірювали, наприклад, концентрацію водних розчинів.
Такий погляд на температуру тримався дуже довго - до кінця XVIII століття. Так і говорили - градуси тепла.
Але одночасно з «речової» теорією теплоти існувала й інша теорія, одним із творців і поборників якої був великий російський вчений М. В. Ломоносов. Ця теорія ґрунтувалася на тому факті, що нагрівання тіла може бути викликано рухом. Ломоносов писав: «Дуже добре відомо, що теплота порушується рухом: від взаємного тертя руки зігріваються, дерево спалахує полум'ям; при ударі кременя про кресало з'являються іскри; залізо розжарюється від проковиванія частими і сильними ударами ... »Звідси робився висновок, що теплота - це не речовина, а рух маленьких частинок, з яких складаються всі тіла (« не чутливі частинок », як їх тоді називали).
Понад двісті років йшла боротьба між цими двома теоріями. Протягом довгого часу панувала перша теорія, але в кінці кінців перемогу здобула друга.
Уже в XVIII столітті були виконані досліди, які змусили багатьох фізиків переглянути уявлення про те, що температура - це концентрація теплоти (теплорода) в тілі.
У 1760 році англійський фізик і лікар Блек показав, що одне і те ж кількість теплоти, підведене до рівних масам різних речовин, призводить до різних змін температури. Але якби температура дійсно представляла концентрацію теплоти в тілі, то отримання одного і того ж кількості теплоти повинно було б викликати у рівних мас будь-яких речовин один і той же зміна температури. У цих дослідах Блек відкрив, як ми тепер знаємо, що у різних речовин різна теплоємність. Але з теорією теплорода це несумісно.
У 1764 році той же Блек показав, що при плавленні льоду їм поглинається значна кількість теплоти, але температура його при цьому залишається незмінною. Цю теплоту з часів Блека часто називають прихованою теплотою плавлення. Точно так же, при твердінні води виділяється теплота і знову - без зміни температури. Ясно, що якщо температура - це концентрація теплоти в тілі, то неможливо поглинання теплоти без підвищення температури і неможлива втрата теплоти тілом без зниження його температури.
Що ж насправді являє собою температура - величина, сенс якої так довго залишався незрозумілим?
Це стало ясним лише після того, як з'явилася кінетична теорія будови речовини. І ми зрозуміємо сенс температури з зіставлення двох нібито зовсім різних речей - одного з результатів кінетичної теорії і способу вимірювання температури.
Про молекулярний хаос і про його законах
Основою кінетичної теорії будови речовини є твердження про те, що будь-яка речовина складається з маленьких частинок - молекул, безперервно і безладно рухаються. Між молекулами діють складні сили тяжіння і відштовхування. Але в газах при звичайних тисках ці сили малі. І можна уявити собі газ, в якому сили взаємодії між молекулами взагалі відсутні. Так як такий газ можна собі лише уявити, то він отримав назву ідеального газу.
Ідеальний газ - це скупчення великої кількості молекул, безладно рухаються в усіх напрямках зі швидкостями в сотні метрів в секунду, раз у раз стикаються між собою і зі стінками посудини. У цьому неймовірному хаосі (можливо, що саме слово газ походить від стародавнього слова хаос) діють, проте, строгі і непорушні закони. Завдяки тому, що в ідеальному газі не треба враховувати сил взаємодії між молекулами, ці закони можна встановити теоретично. Зокрема, можна, користуючись законами механіки, обчислити тиск газу, т. Е. Силу, з якою газ діє на одиницю площі стінки судини. Сила ця є результат ударів рухомих молекул об стінки.
Розрахунок показує, що якщо в посудині об'ємом V знаходиться N молекул газу, то тиск, який чиниться газом на стінки судини, так само
\ (~ P = \ frac 23 \ frac NV \ overline E, \ qquad (1) \)
де \ (~ \ overline E = \ frac {m \ overline {\ upsilon ^ 2}} {2} \) - кінетична енергія хаотичного руху, що припадає в середньому на 1 молекулу газу. Формула (1) показує, що тиск газу дорівнює 2/3 середньої кінетичної енергії хаотичного руху молекул, що містяться в одиниці об'єму (адже \ (~ \ frac NV \) - це якраз і є число молекул в одиниці об'єму).
Для реальних газів розрахунок тиску досить складний, але за певних умов формула (1) досить точна. Вона тим точніше, чим менше величини \ (~ \ frac NV \) і \ (~ \ overline E \). Практично цією формулою можна користуватися при тисках близько 1 атм і менше.
Але яке відношення все це має до температури? Адже в формулу (1) температура не входить!
Щоб це зрозуміти, повернемося до незакінченого нами розгляду способу вимірювання температури.
Про температурних шкалах
Першими термометрами, якими практично користувалися, були рідинні термометри, що виготовлялися групою флорентійських учених. Потім їх стали конструювати і виготовляти і в інших країнах. У них використовувалися різні рідини, але головним чином - спирт і ртуть (іноді масло).
Рідинні термометри представляли собою тонкі скляні трубки, які закінчувалися внизу невеликим кулькою або циліндром. Шарик і нижня частина трубки заповнювалися рідиною (спиртом, ртуттю, маслом). На сторінці 10 ви бачите зразки флорентійських термометрів. (Чи не правда, це не тільки прилади, але і, свого роду, твори мистецтва. Взагалі, за старих часів прилади виготовлялися з «художнім підходом».)
Що стосується термометричні шкал, то використовувалися найрізноманітніші способи їх побудови. Кожен конструктор і виробник термометрів придумував і спосіб створення шкали до них. До кінця XVIII століття в ходу було близько двох десятків різних термометричні шкал, з яких до наших днів збереглися три (що теж дуже багато).
Зрештою переміг принцип побудови термометричні шкал, запропонований голландським склодувом і фізиком-любителем Фаренгейтом і шведським астрономом Цельсієм. Принцип заснований на використанні двох так званих реперних точок, т. Е. Теплових станів, що відрізняються своєю сталістю. Такими точками були температури танення льоду і кипіння води при атмосферному тиску. (Температура плавлення будь-якого твердого речовини і температура кипіння будь-якої рідини при даному тиску також постійні, але вода і лід найбільш доступні.)
У 1742 році Цельсій запропонував такий спосіб градуювання, т. Е. Створення шкали термометрів.
Термометр, який би він не був, наводиться в контакт з тающим льодом, і після встановлення теплової рівноваги рівень рідини в термометрі (якщо це рідинний термометр) відзначається деяким числом. Потім тане лід замінюється киплячою водою, і новий рівень рідини в термометрі відзначається числом, яке відрізняється від першого на 100. А різниця рівнів ділиться на 100 рівних частин - градусів. Зараз здається курйозом, що Цельсій відзначав рівень рідини в термометрі при температурі кипіння води цифрою нуль, а рівень її при температурі танучого льоду - числом 100. Втім, через 8 років, в 1750 році, шкала була перевернута, і в такому вигляді нею користуються і тепер (рис. 2).
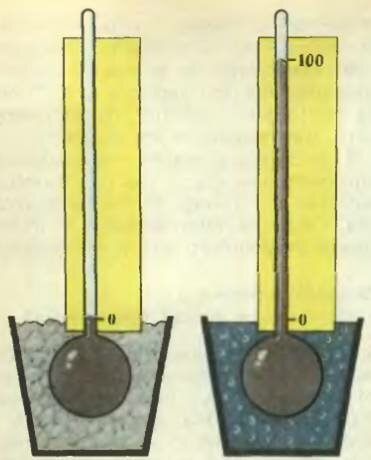
Мал. 2
Ще до Цельсія, в 1724 році, Фаренгейт, теж використовуючи в якості реперних точок температури талого льоду і киплячої води, виготовляв термометри, в яких температура талого льоду відзначалася числом 32, а температура киплячої води - числом 212, так що інтервал температур тане лід - кипляча вода опинявся розділеним не на 100, а на 180 рівних частин - градусів. Французький вчений Реомюр, подібно Цельсієм, приписував температурі танучого льоду значення 0, але по термометру Реомюра вода кипить при температурі 80 градусів.
Як бачимо, в побудові термометричні шкал був чималий свавілля. Довільним було число градусів, на які ділився інтервал температур між крапками реперів. Довільними були і значення температур самих реперних точок. Адже немає розумних підстав вважати, що температура талого льоду дорівнює нулю, т. Е. Що тане лід не має ніякої температури!
Для нас тут важливо, що розділяючи інтервал температур між точками танення льоду і кипіння води на рівні частини (на 100, 80 або 180), ми тим самим вважаємо заздалегідь, що обсяг рідини, якою заповнений термометр, строго лінійно залежить від температури. Якщо позначити обсяг рідини при температурі танучого льоду через V 0, обсяг тієї ж рідини .при температурі киплячої води через V, а самі ці температури через t 0 і t, то розподіл інтервалу температур на рівні частини означає, що
\ (~ \ Frac {V - V_0} {t - t_0} = c, \)
де с - постійна величина. Якщо прийняти, що t 0 = 0, то
\ (~ V = V_0 + ct. \)
Чи можна перевірити, що обсяг справді лінійно залежить від температури? Очевидно, немає. Адже для дослідної перевірки необхідно користуватися термометром. Але при влаштуванні термометра заздалегідь було припущено, що обсяг пропорційний температурі. Тому досвід нічого іншого дати не може.
Існує старий анекдот. В одному морському порту щодня рівно опівдні стріляла гармата. Капітани кораблів, залишаючи порт, перевіряли по гарматного пострілу свої суднові хронометри, за допомогою яких визначають географічну довготу. Один з капітанів побажав дізнатися, наскільки можна бути впевненим в тому, що гармата стріляє дійсно опівдні. І з'ясувалося, що артилерист визначає час по «дуже точним годинах», наявним у місцевого годинникаря. А годинникар сказав капітану, що він перевіряє свої «дуже точний годинник» ... по пострілу портової гармати. Ясно, що при таких умовах не можна судити ні про достоїнства годин, ні про те, чи дійсно рівно опівдні лунає гарматний постріл ...
Для техніки вимірювання температур важливо, що термометри з різними рідинами, а тим більше термометри, в яких про температуру судять не за обсягом рідини, а по яким-небудь іншим властивостям, дають при вимірюванні однієї і тієї ж температури що не збігаються свідчення, причому відмінність в показаннях не однаково в різних температурних областях. У зв'язку з цим виникла необхідність в якомусь стандартному термометрі, за яким градуйованим б все термометри. Тоді їх показання, звичайно, будуть збігатися. Як вирішується це завдання?
В даний час стандартним термометром служить так званий газовий термометр постійного об'єму. Про це термометрі і про нову шкалою температур ми і розповімо.
Газовий термометр і абсолютна шкала температур
У газовому термометрі в якості величини, що залежить від температури, за якою судять про саму температурі, приймається тиск газу в закритій посудині, т. Е. При постійному обсязі. Досвід показує, що тиск нагрітого газу більше, ніж тиск холодного. Сам газовий термометр складається з посудини А, що заповнюється «ідеальним» газом (будь-яким газом при малому тиску), і приєднаного до нього манометра М для вимірювання тиску (рис. 3).
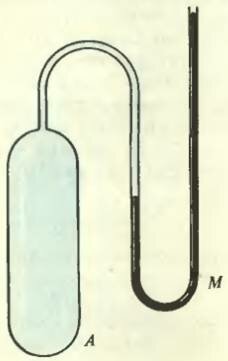
Мал. 3
Якщо посудину помістити в тане лід, а потім в киплячу воду і виміряти значення тисків при цих температурах, забезпечивши теплова рівновага, то виявиться, що тиск при температурі киплячої води в 1,3661 рази більше, ніж при температурі танучого льоду. Якщо позначити тиск і температуру, відповідні киплячій воді, через р і Т, а значення цих величин, відповідні тане льоду, через p 0 і T 0, то
\ (~ \ Frac {p} {p_0} = 1,3661. \ Qquad (2) \)
Щоб не поривати із тепер за двісті років звичної стоградусной шкалою Цельсія, як і раніше вважають, що
\ (~ T - T_0 = 100. \ qquad (3) \)
Різниця тисків при температурах кипіння води і талого льоду ділять на 100 рівних частин - градусів. Це означає, що і тепер ми заздалегідь вважаємо, що температура лінійно залежить від тиску газу при постійному обсязі. Більш того, ми можемо вважати, що температура газу прямо пропорційна його тиску. Перевірити це припущення, зрозуміло, не можна з тієї ж причини, по якій в наведеному вище анекдоті можна по гарматного пострілу перевіряти правильність ходу годинника, а по годинах - своєчасність пострілу. Просто саме вимірювання температури засноване на тому, що тиск газу і його температура вважаються пропорційними один одному. Приписувати температурі танучого льоду значення нуль тепер немає необхідності. Її можна просто обчислити. Справді, якщо температура газу прямо пропорційна тиску, то ставлення тисків газу при температурах окропу і талого льоду дорівнює відношенню самих цих температур, т. Е.
\ (~ \ Frac {p} {p_0} = \ frac {T} {T_0}. \ Qquad (4) \)
Але ставлення, яке стоїть в лівій частині цієї рівності, так само 1,3661. Отже, і права частина дорівнює цьому числу:
\ (~ \ Frac {T} {T_0} = 1,3661. \)
Звідси отримуємо
\ (~ T = 1,3661 T_0. \)
Підставивши це значення для Т в рівність (3), знаходимо
\ (~ 1,3661 T_0 - T_0 = 100, \)
і ми відразу отримуємо
\ (~ T_0 = \ frac {100} {0,3661} \ approx 273,15. \)
Цим і відрізняється нова шкала від шкали Цельсія: температура танення льоду за цією шкалою одно не нулю, а 273,15 градуса. А нуль температури на 273,15 (для стислості на 273) градуси нижче температури танення льоду. Це, як кажуть, абсолютний нуль. Це - та температура, при якій тиск ідеального газу стало б рівним нулю, якщо б така температура була досягнута і якби газ ще залишався при цій температурі газом. Так як тиск газу не може бути менше ніж нуль, то температура на такій шкалі негативною (менше нуля) бути не може.
Описана тільки що температурна шкала (деякі тонкощі в її визначенні, практично несуттєві, ми опускаємо) носить назву абсолютної шкали температур або шкали Кельвіна. І сама температура, яка відлічується по цій шкалі, називається абсолютною температурою. Позначається вона літерою T і виражається в кельвінах (скорочено К), так що температура танення льоду дорівнює 273,15 К, температура кипіння води дорівнює 373,15 К і т. Д.
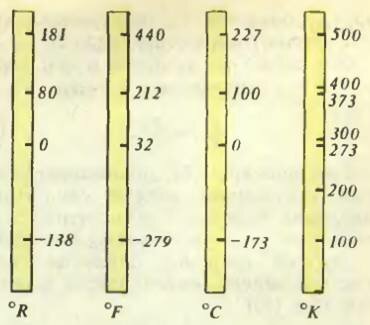
Різні температурні шкали: Реомюра, Фаренгейта. Цельсія і Кельвіна.
Але шкалою Цельсія теж користуються на практиці. Температуру, відлічувану за цією шкалою, позначають буквою t і висловлюють в градусах Цельсія (скорочено ° С). За цією шкалою температура танення льоду дорівнює 0 ° С, температура кипіння води дорівнює 100 ° С і т. Д. Ясно, що
\ (~ T ^ {\ circ} C = (T - 273,15) K. \)
У фізиці майже завжди користуються шкалою Кельвіна.
Тепер нам буде неважко з'ясувати, в чому ж полягає істинний сенс температури.
Що ж таке температура?
Отже, за прийнятим тепер способу вимірювання температури тиск р довільної маси газу М, т. Е. Довільного числа N молекул газу, в посудині об'ємом V пропорційно його абсолютній температурі Т.
Це видно з рівняння (4), яке можна переписати у вигляді
\ (~ \ Frac {p} {T} = \ frac {p_0} {T_0}. \ Qquad (5) \)
Співвідношення (5) показує, що при постійному обсязі відношення тиску газу до його абсолютної температурі - постійна величина. З іншого боку, тиск газу, як ми бачили, визначається формулою (див. (1))
\ (~ P = \ frac 23 \ frac NV \ overline E. \)
Підставивши це значення р в вираз (5), отримуємо
\ (~ T = \ frac 23 \ frac NV \ frac {T_0} {p_0} \ overline E. \ qquad (6) \)
Рівняння (6) відноситься до газу в закритій посудині постійного обсягу. Тому число N молекул газу зберігає постійне значення; відношення \ (~ \ frac {T_0} {p_0} \), як ми бачили, теж постійно. Отже, коефіцієнт при \ (~ \ overline E \) у формулі (6) - постійна величина для будь-якого газу, т. Е.
\ (~ T = \ frac 23 A \ overline E, \ qquad (7) \)
де \ (~ A = \ frac NV \ frac {T_0} {p_0} \) - константа. Це означає, що абсолютна температура газу - це те ж, що середня кінетична енергія хаотичного руху однієї молекули, тільки виражена не в джоулях, а в кельвінах. Коефіцієнт ж \ (~ \ frac 23 A \) - це перекладний множник, який показує, у скільки разів 1 До більше 1 Дж / молекулу. Подібно до цього, одну і ту ж довжину можна виразити в метрах і в дюймах. Необхідно тільки знати, що 1 м = 40 дюйм. Коефіцієнт 40 - перекладний множник, який показує, у скільки разів 1 метр більше 1 дюйма.
Зазвичай формулу (7) записують у вигляді
\ (~ \ Overline E = \ frac 32 kT, \ qquad (8) \)
де
\ (~ K = \ frac 1A = \ frac VN \ frac {p_0} {T_0}. \ Qquad (9) \)
Коефіцієнт k називається постійної Больцмана.
З формули (9) видно, як з досвіду отримати значення постійної Больцмана. Для цього потрібно наповнити посудину відомого об'єму V відомої масою М газу (масу газу можна визначити зважуванням). Потім помістити посудину в тане лід (його температура T 0 = 273,15 К), виміряти за допомогою манометра тиск p 0 газу. Знаючи масу М газу, легко визначити значення N. Дійсно, якщо молярна маса газу μ, то число молей газу одно \ (~ \ frac {M} {\ mu} \); а оскільки в кожному молі газу є N A молекул (N A - число Авогадро), то число молекул N в масі М газу одно \ (~ N = \ frac {M} {\ mu} N_A \). Отже, знаючи масу газу М, його молярну масу μ, обсяг судини V і тиск газу p 0 при температурі T 0, можна визначити значення постійної Больцмана k.
Такого роду вимірювання (а також і багато інших) неодноразово проводилися. Всі вони дають для постійної Больцмана значення
k
= 1,38 · 10-23 Дж / К.
Як ми бачимо, значення k дуже мале. Це означає, що середня кінетична енергія безладних рухів однієї молекули, і яка визначає те, що ми називаємо температурою, надзвичайно мала. При температурі в 1 До середня кінетична енергія молекули \ (~ \ overline E \) дорівнює
\ (~ \ Frac {m \ overline {\ upsilon ^ 2}} {2} = \ frac 32 \ cdot 1,38 \ cdot 10 ^ {- 23} \ approx 2 \ cdot 10 ^ {- 23} \) Дж / молекулу.
Таке співвідношення між Кельвіном і Джоулем на молекулу.
На закінчення нам залишається ще з'ясувати, який зв'язок між температурою і теплотою - двома поняттями, які протягом століть вважалися мало не синонімами.
Відомо, що теплотою називається енергія теплових безладних рухів, що передається від одного тіла до іншого (при теплопередачі). Ясно тому, що теплота не є величиною, що характеризує стан тіла. Про неї не можна сказати, що вона міститься в тілі. Температура ж характеризує стан тіла, тому що вона визначається середньої кінетичної енергією його молекул. Зрозуміло, що між теплотою і температурою по суті ніякого зв'язку немає. Можна тільки сказати, що якщо два тіла мають різну температуру, то вищою є температура того з них, яке передає теплоту іншому. Температура тіла - це величина, яка визначає, чи буде дане тіло віддавати теплоту інших тіл або отримувати її від них. Таке визначення температури свого часу дав Максвелл.
Чи потрібна величина, яка називається температурою?
Температура як поняття і як фізична величина з'явилася в науці задовго до того, як можна було зрозуміти її справжній зміст. Але тепер, коли він відомий, чи варто зберігати цю нібито архаїчну величину? Чи не краще всюди, де ми звикли говорити про температуру, про Кельвіна, про градусах Цельсія, замінити їх тим, що вони є в дійсності - середньої кінетичної енергією частинки, і вимірювати її в джоулях?
Але неважко бачити, що для відмови від температури і від градусів немає підстав.
По-перше, навряд чи буде зручно, наприклад, лікаря вважати пацієнта хворим на тій підставі, що середня кінетична енергія його молекули дорівнює 6,64 · 10-21 Дж, замість того, щоб говорити про температуру в 38 ° С.
По-друге, заміна градусів джоулями може породити і непорозуміння. Адже енергія, наприклад, в 100 Дж, взагалі кажучи, означає, що за її рахунок може бути отримана і робота в 100 Дж. Тим часом якщо температура тіла дорівнює 100 Дж / молекулу (для температури - це фантастичне значення), то це зовсім не значить, що за її рахунок можна отримати таку ж роботу.
Чи потрібна величина, яка називається температурою?Яким же чином температуру все-таки вимірюють?
Але що саме вимірює термометр?
Що таке температура?
Отже, питання про те, що таке температура, зводиться до питання: чим відрізняється холодне тіло від гарячого?
Що ж насправді являє собою температура - величина, сенс якої так довго залишався незрозумілим?
Але яке відношення все це має до температури?
Як вирішується це завдання?
Що ж таке температура?
Чи потрібна величина, яка називається температурою?